- 药品简介
【成份】
本品主要成份为多西他赛,其化学名称为[2aR-(2aα,4β,4aβ,6β,9α,(αR,βS),11α,12α,12aα,12bα)]-β-[[(1,1-二甲基乙氧基)羰基]氨基]-α-羰基苯丙酸[12b-乙酰氧-12-苯甲酰氧-2a,3,4,4a,5,6,9,10,11,12,12a,12b-十二氢-4,6,11-三羟基-4a,8,13,13-四甲基-5-氧代-7,11-亚甲基-1 H-环癸五烯并[3,4]苯并[1,2-b]氧杂丁环-9-基]酯三水合物。
浓溶液:每瓶 0.5 mL:20 mg 注射液相当于 20 mg 多西他赛,溶解于 520 mg 聚山梨酯 80 中而制成。
专用溶剂:浓度为 13%w/w 的注射用乙醇(以 95% 计)水溶液。
每支 20 mg/0.5 mL 注射液含有 20 mg 无水多西他赛,258mg95% 乙醇。
化学结构式:
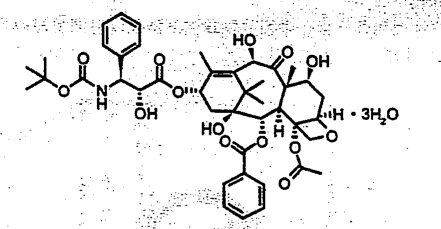
分子式:C43H53NO14·3 H2O
分子量:861.93
本品辅料:浓溶液:聚山梨酯 80(II)、枸橼酸和氮气。溶剂:乙醇和注射用水。
【规格】
0.5 mL:20 mg
【适应症】
乳腺癌:
1. 适用于局部晚期或转移性乳腺癌的治疗。
2. 多西他赛联合曲妥珠单抗,用于 HER2 基因过度表达的转移性乳腺癌患者的治疗,此类患者先期未接受过转移性癌症的化疗。
3. 多西他赛联合阿霉素及环磷酰胺用于淋巴结阳性的乳腺癌患者的术后辅助化疗。
非小细胞肺癌:
适用于局部晚期或转移性非小细胞肺癌的治疗,即使是在以顺铂为主的化疗失败后。
前列腺癌:
多西他赛联合强的松或强的松龙用于治疗激素难治性转移性前列腺癌。
胃癌:
多西他赛联合顺铂和 5-氟尿嘧啶(TCF 方案)用于治疗既往未接受过化疗的晚期胃腺癌,包括胃食管结合部腺癌。
【警告】
中毒性死亡、肝毒性、中性粒细胞减少、超敏反应、体液潴留 1. 在具有肝功能异常的患者,接受高剂量治疗的患者,以及既往使用过铂类为基础的化疗再接受多西他赛单药100mg/m2治疗的患者中,治疗相关死亡的发生率增加。 2. 对于出现胆红素>正常值(ULN)上限的患者,或者天门冬氨酸氨基转移酶(AST)和/或丙氨酸氨基转移酶(ALT)>1.5×ULN合并碱性磷酸酶>2.5×ULN的患者,应该避免使用多西他赛。存在胆红素升高或转氨酶异常伴碱性磷酸酶升高的患者发生4级的中性粒细胞减少,发热性中性粒细胞减少,感染,严重的血小板减少,严重胃炎,严重皮肤毒性以及中毒性死亡的风险更高。仅存在转氨酶>1.5×ULN的患者4级的中性粒细胞减少发生率更高,但中毒性死亡的发生率不高。因此,在每个周期开始给予多西他赛之前应进行胆红素、AST或ALT以及碱性磷酸酶检查。 3. 中性粒细胞计数<1500个/mm3的患者应避免给予多西他赛。为了监测中性粒细胞减少的发生以免其发展至严重程度导致感染,应对所有接受多西他赛治疗的患者进行频繁的血细胞计数。 4. 在接受了3天的地塞米松预治疗的患者,报道了严重过敏反应,表现为全身性皮疹/红斑,低血压和/或支气管痉挛,或非常罕见的致命性过敏症。一旦发生,应立即停药并给予适当的救治。既往有对多西他赛或其他含聚山梨酯-80制剂严重过敏史的患者应避免使用。 5. 在接受了3天的地塞米松预治疗的患者中有6.5%(6/92)报道严重的体液潴留。表现为以下一种或多种事件:不能耐受的外周水肿,全身性红斑,心脏压塞,需要积极引流的胸腔积液,呼吸困难,明显的腹部膨胀(因为腹水)。
【药理作用】
多西他赛为抗肿瘤药,通过促进小管聚合成稳定的微管并抑制其解聚从而使游离小管的数量显著减少。多西他赛与微管的结合不改变原丝的数目。
体外实验表明,多西他赛可以破坏微管网状结构,该结构对处于有丝分裂间期的细胞的功能具有重要作用。
体外实验证明,多西他赛对多种小鼠及人体肿瘤细胞株有细胞毒作用。另外,在克隆形成实验中,对新切除的人体肿瘤细胞也有细胞毒作用。多西他赛在细胞内浓度高且潴留时间长。此外,对过度表达 P-糖蛋白(由多药耐药基因编码)的许多肿瘤细胞株具有活性。体内实验中,多西他赛抗瘤谱广,对晚期小鼠和人移植性肿瘤均具有抗肿瘤活性,且与用药方案无关。
【药代动力学】
在 I 期研究中,对癌症患者进行了剂量为 20-115 mg/m2的多西他赛药代动力学研究。多西他赛的药代动力学特点与剂量无关,符合三室药代动力学模型,α,β,γ半衰期分别为 4 分钟、36 分钟及 11.1 小时。后一时相部分原因是由于药物从周边室相对缓慢地消除。在 1 小时内静脉输注给予多西他赛 100 mg/m2,平均峰浓度为 3.7 μg/mL,AUC 为 4.6 h•μg/mL,总体清除率和稳态分布容积分别为 21L/h/m2与 113L。机体总清除率的个体差异约为 50%。多西他赛的血浆蛋白结合率超过 95%。
多西他赛及其代谢产物主要从粪便排泄。经粪便和尿排出的量分别约占所给剂量的 75% 和 6%,仅有少部分以原型排出。体外研究表明,细胞色素 P450-3A 同工酶与多西他赛的代谢有关,多西他赛的蛋白结合率超过 95%,地塞米松并不影响多西他赛与蛋白的结合。
在3 例癌症患者中进行了14C-多西他赛研究,多西他赛以细胞色素 P450-介导的 3-丁基酯氧化代谢产物从尿及粪便排泄。7 日内,尿和粪便排出分别约占所给放射物的 6% 和 75%,在前 48 小时约 80% 放射物在粪便中被发现,包括 1 种主要非活性代谢物及 3 种微量非活性代谢物以及极少量的原型药物。
多西他赛群体的药代动力学分析在 577 例患者中进行。通过模型评估的药代动力学参数与 I 期临床研究结果非常接近。多西他赛的药代动力学与患者的年龄或性别无关。在少量患者(n = 23)的临床生化数据结果表明,轻至中度肝功能损伤(ALT,AST ≥ 1.5 倍 ULN 伴有碱性磷酸酶 ≥ ULN2.5 倍)时,总清除率平均降低 27%。(见《用法用量》)。多西他赛清除率在轻至中度体液潴留的患者中无变化,尚无在重度体液潴留患者中用药的数据。
在联合用药中,多西他赛不影响阿霉素的清除率及阿霉素醇(阿霉素的代谢产物)的血浆浓度。在 30 例乳腺癌患者中研究发现,同时服用多西他赛、阿霉素和环磷酰胺不会影响它们药代动力学特性。
I 期研究评估了卡培他滨与多西他赛,结果显示卡培他滨不影响多西他赛(Cmax及 AUC)药代动力学特性,多西他赛也不影响卡培他滨有关代谢物 5-DFUR 的药动学特性(卡培他滨最主要的代谢产物)。
在联合顺铂或卡铂时,多西他赛清除率与单一用药时相似。当多西他赛输注后紧接顺铂治疗,顺铂的药代动力学特性与其单一用药时相似。
12 例患者使用多西他赛联合顺铂与 5-氟尿嘧啶治疗实体瘤药代研究结果显示,联合用药不影响每个药物的药代动力学。
42 例患者使用标准地塞米松预防用药,研究强的松对多西他赛药代动力学的影响。未观察到强的松对多西他赛药代动力学产生影响。
【毒理研究】
致癌作用
多西他赛的致癌性没有研究。
致突变作用
多西他赛在 CHO-K1 细胞的体外微核及染色体畸变实验中,及小鼠体内微核实验中表现出有致突变现象。然而,在 Ames 实验中或在 CHO/HGPRT 基因突变实验中没有致突变性。本结果与多西他赛的药理学活性是一致的。
对生殖能力的损伤
啮齿动物毒性实验中的不良反应显示多西他赛可能减弱雄性的生育能力。
【上市许可持有人】
江苏恒瑞医药股份有限公司
【生产企业】
江苏恒瑞医药股份有限公司
信息来源:丁香园用药助手